日本の化粧品表示規制の理解
化粧品およびパーソナルケア製品を日本市場に導入する上で、適切な表示は極めて重要です。日本の化粧品規制は消費者安全を確保し、公衆とブランド双方を保護するための厳格なコンプライアンス要件を定めています。誤解を招く表示や不正確な表示は、多大な遅延、法的問題、市場アクセス喪失につながる可能性があります。本ガイドでは、日本の化粧品表示規制を解説し、この市場での成功を目指す国際ブランド向けに実践的なガイダンスを提供します。
詳細はこちら:日本における化粧品・パーソナルケア製品の主要輸入規制
日本の化粧品表示規制
日本の化粧品市場は世界第4位の規模を誇り、約3,000社が参入する中でスキンケアが主力分野となっている。この成長は高品質で革新的、かつ環境に配慮した製品への需要増加に支えられており、日本の厳格な化粧品規制への準拠が重要であることを示している。
この業界は、以下の主要な規制機関および法律によって管理されています:
- 厚生労働省(MHLW):
化粧品及び個人用ケア製品の規制枠組みを監督する。 - 医薬品医療機器総合機構(PMDA):
厚生労働省の下で、輸入申請および製品承認の審査を行う。
日本では透明性と消費者安全を確保するため、表示義務が定められています。全ての表示は日本語で記載され、外装には完全な原材料リストを記載しなければなりません。これらの規制は、消費者が購入する製品について正確かつ明確な情報を得られるようにすることで、消費者を保護することを目的としています。
必須表示事項
日本の規制で要求される主要な表示要素には以下が含まれます:
パターン1:内積パッケージのみ
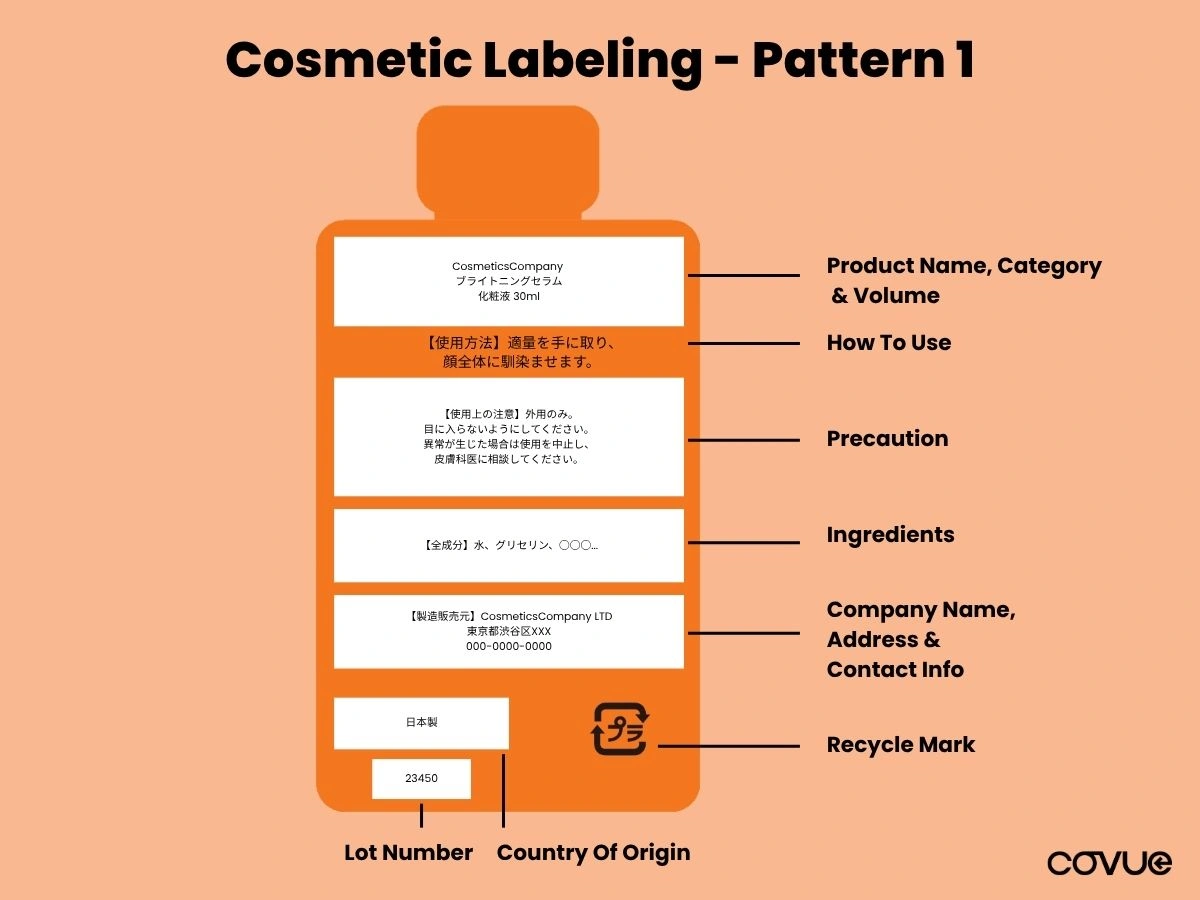
製品包装が製品全体であり、外装が含まれない場合。製品には以下の項目を含める必要があります:
- 製品名:製品の正式名称。
- 製品カテゴリー:分類(例:ローション、クリーム、シャンプーなど)
- 容量:内容量(ミリリットル(ml)またはグラム(g)で表示)。
- ユーザーマニュアル:基本的な使用方法のガイド。
- 成分表示:すべての成分は濃度が高い順に記載され、日本語で表記され、厚生労働省が指定する成分表示形式に準拠しなければならない。
- 注意事項:保管および使用に関する警告または重要な安全情報。
- 会社名(化粧品製造販売業者):市場における製品に対する法的責任を負う法人。
- 会社住所(化粧品製造販売業許可証保持者):追跡可能性のための許可証保持者の完全な住所。
- 連絡先情報(ウェブサイトまたは電話番号):任意ですが、消費者サポートのため推奨されます。
- 原産国:製品の製造国を明記すること。
- ロット番号:リコールや問題発生時の製品追跡可能性のため。
- 製造年月日/消費期限:必須ではありませんが、包装に記載することをお勧めします。
- リサイクルマーク:日本のリサイクル基準に沿った正しい廃棄方法を表示してください。
パターン2:外箱包装付き
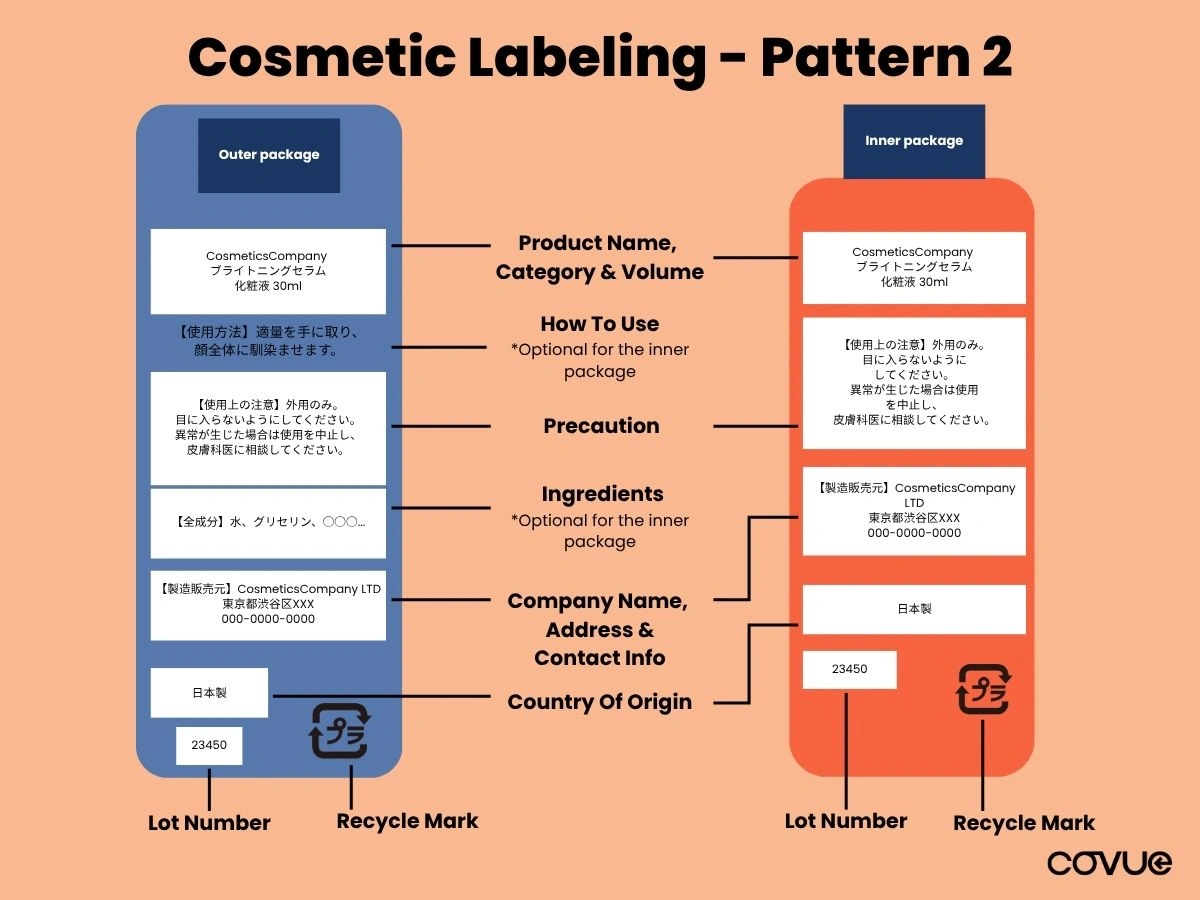
製品に外装と内装の両方がある場合(例:箱に入ったボトル)。包装には以下の項目を記載する必要があります:
| ラベル項目 | 外装 | 内包装 |
| 製品名 | ✅ | ✅ |
| 製品カテゴリー | ✅ | ✅ |
| 体積(ml/g) | ✅ | ✅ |
| ユーザー操作手順 | ✅ | – |
| 原材料リスト | ✅ | – |
| 注意事項 | ✅ | ✅ |
| 会社名(化粧品製造販売業許可証保持者) | ✅ | ✅ |
| 会社住所(化粧品製造販売業許可証保持者) | ✅ | ✅ |
| 連絡先情報(任意) | 任意 | 任意 |
| 原産国 | ✅ | ✅ |
| ロット番号 | ✅ | ✅ |
| 製造年月日/使用期限 | 任意 | 任意 |
| リサイクルマーク | ✅ | ✅ |
ラベル書式設定 要件
化粧品製品のラベルは、以下の要件に従わなければなりません:
- フォントサイズ:最小7ポイント。スペースが限られている場合は4.5ポイントでも可。
- 小容量包装の例外:30ml以下の容器は、文字サイズに関する規則の適用除外となります。
- 容量表記:ミリリットル(ml)またはグラム(g)で明確に表示すること。
- 明瞭で読みやすい日本語フォントの使用を強く推奨します。
他製品カテゴリーとの差異
化粧品は表示の点で食品、サプリメント、医薬品と共通点を持つ一方で、顕著な相違点がある:
- 化粧品:表示は厳格な規制に従わなければならず、特に安全性及び有効性に関する表示が対象となる。治療効果を主張する表示は、製品が医薬部外品に分類されない限り、一般的に禁止されている。
- 食品とサプリメント:食品には栄養成分表示とアレルゲン表示が必須であり、サプリメントは健康表示規制に準拠する場合に限り健康効果を主張できる。これらのカテゴリーでは原材料表示も義務付けられるが、より重点が置かれるのは栄養成分である。
- 医薬品:医薬品は特定の治療効果を主張できますが、厚生労働省および医薬品医療機器総合機構(PMDA)の承認が必要です。また、ラベルには用法用量および医療上の警告を記載しなければなりません。
主な違いは、化粧品は医薬部外品に分類されない限り、治療効果や薬効を主張できない点である。さらに、主張を行う医薬部外品については、有効成分に基づき厚生労働省の承認が必要となる。厚生労働省が製品の有効性を認めるため、こうした製品はしばしば「薬用化粧品」と呼ばれる。
一般的な表示コンプライアンス上の課題
多くの国際ブランドが、日本の化粧品表示規制への対応において課題に直面している:
- 虚偽の主張:製品の安全性や有効性について承認されていない主張を行うと、却下や罰金につながる可能性があります。
- 原材料表示の誤り:原材料を正しい順序で表示しない、または重要な原材料を記載しないことは、遅延の原因となる可能性があります。
- 表示言語の問題:日本語表示が義務付けられているため、誤った翻訳や不完全な翻訳はコンプライアンス上の問題を引き起こす可能性があります。
- 誤った主張:「医師推奨」や「臨床的に証明済み」といった主張は、厚生労働省の承認がない限り禁止されています。
非準拠は輸入遅延、罰金、あるいは市場からの撤退につながる可能性があります。
コンプライアンスを確保する方法
日本市場への円滑な参入と化粧品表示規制への準拠を確保するため、ブランドは以下のベストプラクティスを検討すべきです:
- 専門家への相談:日本の法律や要件を理解している規制の専門家と連携する。
- プロの翻訳者を利用してください:製品のラベルが正確に日本語に翻訳され、混乱や誤りを防ぐようにしてください。
- 市場投入前チェックの実施:市場投入前チェックは、承認申請書類を提出する前に、製品およびラベルがすべての必要な規制に準拠していることを確認するのに役立ちます。
- 最新情報を入手:規制は変化する可能性があるため、日本の表示要件の変更について常に情報を得ておくことが、継続的なコンプライアンス維持に不可欠です。
日本では、化粧品の表示は最終包装工程ではない。製品が合法的に市場に参入し、流通し続けられるかどうかを決定する規制上のゲートキーパーである。
製造、印刷、または出荷を開始する前に、ブランドは日本の医薬品医療機器等法(PMD法)の枠組みのもとで、成分表示、効能・効果の表示、医薬部外品の分類、および認可構造を整合させなければならない。






